- Почки
Почки (renes) — парный экскреторный и инкреторный орган, выполняющий посредством функции мочеобразования регуляцию химического гомеостаза организма.
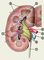
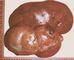
Почки расположены в забрюшинном пространстве на уровне XI грудного — III поясничного позвонков. Правая почка более подвижна и располагается несколько ниже левой почки имеют бобовидную форму. Масса каждой почки в норме составляет 120—200 г, длина 10—12 см, ширина — 5—6 см, толщина — 3—4 см. Каждая почка состоит из наружного (коркового) и внутреннего (мозгового) слоев; мозговое вещество представлено пирамидами, основания которых обращены в сторону коры, а верхушки открываются в почечную лоханку (рис. 1). Кровоснабжение почек обеспечивают почечные артерии, отходящие от брюшной аорты и разделяющиеся в воротах каждой почки на две главные артерии — переднюю и заднюю. Отток крови от каждой почки происходит по почечной вене, впадающей в нижнюю полую вену.
Иннервируются почки волокнами почечного нервного сплетения, образованного ветвями чревного сплетения, блуждающего нерва, конечными ветвями чревных нервов, ганглиозными клетками.
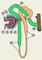
Основной структурно-функциональной единицей почки является нефрон, состоящий из нескольких отделов (рис. 2), выполняющих различные функции. Нефрон включает почечный клубочек капиллярных петель, расположенных между приносящей и выносящей артериолами, заключенных в капсулу Шумлянского — Боумена, проксимальный каналец; петлю Генле; дистальный каналец, впадающий в собирательную трубочку. Последняя завершает систему канальцев и морфологически уже не относится к нефрону. Между приносящей и выносящей артериолами клубочка расположен юкстагломерулярный комплекс, в т. ч. клетки, секретирующие ренин — фермент подкласса протеиназ, катализирующий превращение ангиотензиногена в ангиотензин. В каждой почке содержится 1—1,2 млн. нефронов, из которых приблизительно 85% являются кортикальными, а 15% расположены на границе с мозговым веществом почки. Последние, юкстамедуллярные нефроны, принимают непосредственное участие в процессах осмотического концентрирования мочи.
Важнейшая физиологическая роль почек — гомеостатическая: почки участвуют в поддержании постоянства концентрации осмотически активных веществ в плазме и межклеточной жидкости (осморегуляция), их объема (волюморегуляция), электролитного и кислотно-основного баланса, экскретируют продукты азотистого обмена, принимают участие в процессах метаболизма белков, углеводов, липидов, в превращении и выделении из организма токсических веществ, в регуляции системной гемодинамики. Большинство перечисленных функций почек обеспечиваются процессами образования мочи: клубочковой фильтрацией (ультрафильтрацией), реабсорбцией части ультрафильтрата (пассивной и активной), секрецией в канальцах различных веществ и синтезом новых соединений. Почки осуществляют также инкреторную функцию, синтезируя ряд биологически активных субстанций (эритропоэтин, ренин, активный витамин D3, простаглаидины и пр.).
Процесс образования мочи начинается с клубочковой фильтрации, величина которой зависит от ряда гемодинамических факторов, прежде всего от объема почечного кровотока, который регулируется главным образом вазоактивными субстанциями (адреналин, ангиотензин, простагландины, брадикинин и др.), симпатическими нервами, гормонами. Почки содержат большое количество кровеносных сосудов, общее сопротивление которых невелико, поэтому в почки ежеминутно поступает около 25% сердечного выброса.
Тотальный почечный кровоток у взрослого человека составляет примерно 1200 мл в 1 мин в пересчете на стандартную поверхность тела (1,73 м2). Из этого объема крови 91—93% протекает по сосудам коркового вещества почек (эффективный почечный кровоток). В наружное мозговое вещество поступает около 6—8%, а во внутреннее — менее 1% объема крови. Основное сопротивление кровотоку оказывают капилляры почечного клубочка, динамика сопротивления определяется тонусом приносящих и выносящих артериол. Изменение давления в почечной артерии сопровождается реактивным изменением тонуса приносящей артериолы клубочка, за счет чего поддерживаются постоянный почечный кровоток и капиллярное давление в клубочке (саморегуляция).
Процесс образования мочи начинается с ультрафильтрации через клубочковый фильтр в просвет капсулы клубочка плазменной воды и растворенных в ней различных веществ с малой молекулярной массой (электролитов, органических соединений). Скорость клубочковой фильтрации в обеих почках составляет в среднем 120 мл в 1 мин — примерно 100 л в сутки на 1 м2 поверхности тела. Фильтрация в клубочках обеспечивается фильтрационным давлением — разностью между гидростатическим давлением в капиллярах гломерул (45—52 мм рт. ст.). с одной стороны, и онкотическим давлением плазмы крови (18—26 мм рт. ст.) и гидростатическим давлением в полости капсулы Шумлянского — Боумена (8—15 мм рт. ст.) — с другой. В норме фильтрационное давление колеблется в пределах 10—20 мм рт. ст. Клубочковая фильтрация снижается при уменьшении системного АД (она прекращается при значениях АД ниже 50 мм рт. ст.), при повышении давления в канальцах и, соответственно, в капсуле клубочка (вследствие затруднения оттока мочи, при повышении давления в интерстиции почки). Регуляция скорости клубочковой фильтрации в каждом нефроне осуществляется объемом протекающей крови и скоростью реабсорбции натрия в данном нефроне. Этот процесс протекает при участии юкстагломерулярного комплекса, реагирующего на растяжение приносящей артериолы притекающей кровью и на квоту реабсорбции натрия в канальце. Секреция ренина, возрастающая при уменьшении растяжения артериолы, активирует превращение ангиотензиногена в ангиотензин, что приводит к повышению АД, увеличению почечного кровотока и клубочковой фильтрации, стимулирует рефлекс жажды.
Состав ультрафильтрата (первичной мочи) изменяется в процессе пассажа по системе канальцев, где при участии ферментов, содержащихся в клетках тубулярного эпителия, происходит транспорт веществ через стенку канальцев благодаря процессам реабсорбции (вещество переходит из просвета канальца в интерстиции) и секреции (транспорт вещества идет в противоположном направлении). Транспорт веществ через стенку канальца осуществляется с затратой энергии. Различают активный транспорт — перемещение молекул против электрохимического или концентрационного градиента и пассивный транспорт (диффузию) — перемещение молекул вещества по электрохимическому градиенту, создаваемому путем активного транспорта других веществ.
В проксимальном отделе нефрона реабсорбируется почти полностью профильтровавшийся белок, аминокислоты, глюкоза и большая часть солей. В канальцах и собирательных трубках происходят последующие процессы всасывания и секреции веществ, определяющие окончательный состав выделяемой мочи.
Экскреция белка с мочой в норме не превышает 50 мг в сутки. Увеличение фильтрации белка при поражении клубочков или недостаточная его реабсорбция в проксимальных канальцах могут быть причиной протеинурии.
Поступающие с фильтратом аминокислоты почти полностью подвергаются реабсорбции в проксимальном отделе нефрона. В почках происходят также трансаминирование и дезаминирование аминокислот и расщепление некоторых пептидов (ангиотензин II, брадикинин, инсулин и др.) до аминокислот с последующим их всасыванием в кровь. Увеличение экскреции аминокислот с мочой (аминоацидурия) наблюдается при ускоренной их фильтрации или дефиците ферментов, участвующих в метаболизме и реабсорбции отдельных аминокислот.
Суточная экскреция глюкозы в норме не превышает 130 мг. Реабсорбция глюкозы связана с работой натриевого насоса, удаляющего натрий из клетки через плазматическую мембрану. Количественная оценка показателей реабсорбции глюкозы позволяет судить о функциональном состоянии проксимального сегмента канальцев, а также о количестве эффективно работающих нефронов. Экскреция глюкозы с мочой начинается лишь при условии, что количество профильтровавшейся глюкозы превышает реабсорбционную возможность канальцев. Чаще всего наблюдается при гипергликемии. В норме максимальный транспорт глюкозы у мужчин составляет 375±79,7 мг в 1 мин, у женщин — 303±55,3 мг в 1 мин на 1,73 м2 поверхности тела. У больных сахарным диабетом глюкозурия может уменьшаться, несмотря на стабильно высокий уровень гипергликемии. Это обусловлено прогрессирующим гломерулосклерозом, снижением скорости КФ и, соответственно, уменьшением нагрузки канальцев глюкозой.
Осморегулирующая функция почек связана с процессами реабсорбции ионов натрия и хлора. Активная реабсорбция ионов хлора происходит в толстом восходящем отделе петли нефрона, где функционирует хлорный насос. Ионы натрия реабсорбируются здесь пассивно. Этот участок канальца непроницаем для воды. Фуросемид и этакриновая кислота оказывают свое действие только при попадании в просвет канальца, где они блокируют реабсорбцию хлора и тем самым пассивную реабсорбцию натрия, повышая натрийурез. В извитой части дистального канальца функционирует натриевый насос, реабсорбция хлора происходит пассивно. Отдел дистального нефрона, предшествующий собирательной трубочке, обладает свойством изменять свою проницаемость для воды под влиянием антидиуретического гормона. Функция натриевого насоса регулируется альдостероном. В этом сегменте нефрона реализуется действие спиронолактона, триамтерена и амилорида. Спиронолактон снижает реабсорбцию натрия. Амилорид и триамтерен блокируют вход натрия в клетки данного участка канальцев, и нереабсорбируемый натрий выделяется с мочой.
Экскреция калия составляет примерно 10% от количества фильтрующегося калия. Профильтровавшийся в клубочках калий почти полностью реабсорбируется и затем секретируется в извитой части дистального канальца и собирательных трубках в обмен на натрий. Альдостерон и сердечные гликозиды снижают реабсорбцию калия. Секреция калия стимулируется альдостероном (повышает проницаемость мембран клеток канальца для ионов калия, облегчая пассивный выход их из клетки), тормозится инсулином, антагонистами альдостерона. Кроме этого, выделение калия с мочой зависит от кислотно-щелочного состояния, при этом алкалоз способствует усилению калийуреза, ацидоз его снижает.
Осмотическое концентрирование и разведение мочи осуществляются путем функционирования петли нефрона и собирательных трубочек как «противоточного умножителя»: противонаправленное движение первичной мочи в петле нефрона и в собирательных трубках, по-разному проницаемых для воды и натрия, обусловливает возможность уравновешивания концентрации осмотически активных веществ в моче и интерстиции почек посредством пассивного движения воды по осмотическому градиенту. Последний создается благодаря активному транспорту хлорида натрия в интерстиции из толстого отдела восходящего колена петли нефрона, непроницаемого для воды, и обеспечивает движение воды из просвета нисходящего колена петли нефрона, стенка которого для воды проницаема.
Регуляция почками кислотно-щелочного равновесия осуществляется главным образом путем реабсорбции бикарбоната натрия и секреции ионов водорода в виде различных кислых соединений (хлорида аммония, однозамещенного фосфата и др.). В норме суточная экскреция ионов Н+ с мочой составляет 50—70 ммоль.
Инкреторная и метаболическая функции почек играют важную роль в гуморальной регуляции ряда физиологических процессов в организме. Кроме секреции ренина почки участвуют в промежуточном обмене ряда гормонов, в частности в катаболизме инсулина, антидиуретического гормона. АКТГ, ангиотензина, гастрина, в превращении витамина D в его наиболее активную форму — 1,25-дигидроксихолекальциферол (витамин D3), а также в синтезе и секреции ряда биологически активных веществ, в т. ч. простагландинов Е2 и F2, а также некоторых кининов, увеличивающих кровоток и стимулирующих натрийурез. В почках синтезируются вещества, регулирующие эритропоэз. Среди этих веществ выделяют эритрогенин, активирующий печеночный эритропоэтиноген, в результате чего в крови появляется эритропоэтин; возможна также секреция почками проэритропоэтина. Почки принимают участие в процессах свертывания крови. В них вырабатывается урокиназа, происходит метаболизм гепарина и продуктов деградации фибрина. Метаболическая функция почек определяется также их участием в синтезе глюкозы (почечный глюконеогенез), окислении свободных жирных кислот, синтезе фосфолипидов.
Возрастные особенности физиологии почек характеризуются относительно медленным становлением гомеостатической функции почек у детей и постепенным ее снижением у лиц пожилого возраста.
У новорожденных фильтрующая поверхность клубочковых мембран, их проницаемость, а также фильтрационное давление в клубочках меньше, поэтому и скорость клубочковой фильтрации в расчете на 1 м2 поверхности тела существенно меньше, чем у взрослых. В возрасте 6 месяцев отношение клубочковой фильтрации к поверхности тела способно достигать значений, близких к таковым у взрослых, но стабилизируется на этих значениях лишь на третьем году жизни ребенка. Канальцевая реабсорбция и секреция у новорожденных также ограничены, что в немалой степени обусловлено сниженной чувствительностью эпителия канальцев к действию регулирующих гормонов. Для выведения из организма осмотически активных веществ ребенку необходимо больше воды, чем взрослому человеку. К подростковому периоду чувствительность почек к действию антидиуретического гормона, альдостерона, вазопрессина и других гормонов становится почти такой же, как у взрослых, и диапазон приспособительных реакций почек на осмотическую и другие нагрузки существенно расширяется.
Инволютивные изменения почек начинаются на четвертом десятилетии жизни. К 70 годам популяция нефронов сокращается нередко более чем наполовину, чему в ряде случаев способствуют склеротические изменения артериол и интерстиция почек, особенно в области почечных сосочков. Структурные изменения почек сопровождаются нарушением почечных функций: уменьшается скорость клубочковой фильтрации, снижается концентрационная способность, ограничивается способность поддержания водно-электролитного и кислотно-щелочного баланса, что особенно проявляется при операционных вмешательствах, инфекциях, дегидратации. В старческом возрасте изменяется структура заболеваний почек ; реже встречаются острый и подострый нефрит, поражения почек при системных заболеваниях, но чаще отмечаются хронический пиелонефрит, диабетический гломерулосклероз, амилоидоз почек, паранеопластические нефропатии.
МЕТОДЫ ИССЛЕДОВАНИЯ И СЕМИОТИКА
Для диагностики заболеваний почек используют как основные методы обследования больного — анамнез, осмотр больного, пальпацию и аускультацию почек (см. Обследование больного), так и многообразные специальные методы исследования морфологии и функции почек, среди которых к обязательным относятся лабораторные анализы мочи. Из основных методов специальных навыков требуют аускультация почечных артерий (см. Сосудистые шумы) и пальпация почек.
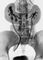
Пальпация почек производится бимануальным методом (рис. 3). Положение больного — лежа со слегка приподнятой головой. Находясь справа от больного, врач располагает ладонь левой руки на пояснице больного (кончики пальцев руки должны касаться m. erector spinae), ладонь правой руки — на передней брюшной стенке (кончики пальцев должны быть направлены к краю реберной дуги). Больному предлагают расслабить мышцы живота и сделать глубокий вдох. Во время вдоха правую руку следует постепенно погружать в глубь живота, а левой рукой оказывать давление на область поясницы. Во время вдоха происходит некоторое смещение почки вниз, в результате чего ее удается пальпировать и оценить ее форму, величину, характер поверхности, болезненность, плотность, смещаемость. Если состояние больного позволяет, желательно произвести пальпацию почек в положении больного стоя. При этом пациент должен стоять лицом или вполоборота к врачу, сидящему на стуле. Мышцы брюшного пресса должны быть расслаблены, а туловище слегка наклонено вперед. В норме почка имеет плотную (но не твердую) консистенцию, гладкую поверхность.
Исследования мочи начинают с ее общего анализа, характеризующего основные физико-химические свойства и микроскопический состав осадка мочи. Для исследования желательно собрать утреннюю концентрированную мочу, ее среднюю порцию. Микроскопию мочевого осадка следует производить не позднее 2 ч после сбора мочи, а при низкой относительной плотности мочи (менее 1010) — непосредственно после ее сбора.
Свежевыпущенная моча в норме прозрачна, имеет соломенно-желтый цвет. При полиурии и хронической почечной недостаточности окраска мочи менее интенсивная, а при повышенном катаболизме белков (лихорадка, гипертиреоз, инфекция, опухоли) она более насыщенна. Помутнение мочи может быть следствием высокого содержания солей, лейкоцитов, бактерий. Реакция мочи обычно кислая. Щелочная реакция мочи наблюдается при безмясном пищевом рационе, богатом фруктами, овощами; стойкое повышение рН мочи может быть признаком почечного канальцевого ацидоза, бактериальной инфекции, способной разлагать мочевину до аммония. В кислой моче легко образуются кристаллы из уратных и оксалатных солей, в щелочной — из фосфатных солей.
Протеинурия у здоровых лиц качественными пробами обычно не определяется, а за сутки она не превышает 50 мг. Качественные реакции на белок (пробы с сульфосалициловой и азотной кислотами) становятся положительными при содержании в моче белка от 0,033 г/л и более. Для диагностики и оценки тяжести поражения почек более информативно определение суточной протеинурии, чем содержания белка в разовых анализах мочи. Качественный состав белков мочи анализируется по их молекулярной массе, иммунохимическим свойствам. С этой целью используются электрофорез в крахмальном или полиакриламидном геле, гель-хроматография, иммуноэлектрофорез. Наиболее точен метод гель-фильтрации на сефадексе.
Микроскопия мочевого осадка позволяет обнаружить эритроциты, лейкоциты, цилиндры, клетки эпителия. У здоровых людей в поле зрения микроскопа при 40-кратном увеличении встречаются 1—2 эритроцита и лишь в отдельных анализах число лейкоцитов обычно не превышает 5 в поле зрения; иногда выявляются единичные гиалиновые цилиндры (например, после физической нагрузки), зернистые и восковидные цилиндры в норме никогда не обнаруживаются.
Общий анализ мочи дает ориентировочное представление о степени лейкоцитурии, эритроцитурии. Более точная их оценка достигается при определении числа клеток в стандартном объеме (в 1 мл мочи по Нечипоренко) или за конкретное время (за сутки — метод Каковского — Аддиса, за минуту — метод Амбюрже). Метод Нечипоренко широко применяется в клинической практике в связи с простотой исследования (анализируется средняя порция свежевыпущенной мочи). Однако в пробе Нечипоренко не учитываются суточные колебания лейкоцитурии, которые могут быть весьма значительными.
Бактериоскопическое исследование осадка мочи является ориентировочным тестом для выявления грибков и диагностики туберкулеза мочевой системы (микроскопия мазков из осадка мочи с окраской по Цилю — Нильсену). Более надежны для диагностики туберкулеза почек бактериологического исследования мочи по методу Прейса — Школьниковой и особенно биологический метод — подкожная инъекция мочи больного морской свинке с целью ее заражения. Наиболее важное значение имеет посев мочи с количественной оценкой степени бактериурии (метод Гоулда). О диагностическом значении бактериурии говорят при обнаружении в 1 мл мочи более 105 возбудителей.
Исследование функционального состояния почек основано главным образом на клиренс-тестах (см. Клиренс) и состоит в определении скорости клубочковой фильтрации (клиренс эндогенного креатинина), клиренса мочевины, эффективного почечного плазмотока, а также экскреции аминокислот, глюкозы, фосфатов, натрия, способности к осмотическому разведению и концентрированию мочи, скорости экскреции аммония, титруемых кислот, водородных ионов, способности к ацидификации мочи. Минимальный комплекс исследований включает определение скорости клубочковой фильтрации, оценку концентрационной функции почек по относительной плотности мочи в одиночном анализе, в пробе Зимницкого или пробе с сухоядением, а также исследование способности почек к ацидификации мочи.
Для определения скорости клубочковой фильтрации по клиренсу эндогенного креатинина необходимо собирать мочу в течение 24 ч с точностью до 1 мин. Клиренс эндогенного креатинина (С) определяют по формуле:
![]() ,
,
где U и Р — концентрация креатинина соответственно в моче и плазме крови, V — величина минутного диуреза. Реже скорость клубочковой фильтрации исследуют с помощью клиренсов радиоактивных изотопов, используя для этой цели этилендиаминтетраацетат, иоталамат натрия, меченный радиоактивным хромом. Величина клубочковой фильтрации в физиологических условиях колеблется в зависимости от возраста, психической и физической нагрузки, характера питания, количества употребляемой воды в разное время суток и др. Наименьшие ее значения отмечаются ранним утром и ночью, наибольшие — днем. Начиная с 40-летнего возраста величина клубочковой фильтрации снижается примерно на 1% в год.
Концентрационную функцию почек можно ориентировочно оценить по показателю относительной плотности утренней мочи, составляющему в норме не менее 1018. Учитывают, что у больных с выраженной глюкозурией этот показатель повышается примерно на 4 на каждый 1% сахара в моче, а у больных с протеинурией — на 1 на каждые 3 г/л белка. После применения рентгеноконтрастных веществ относительную плотность мочи следует определять спустя 1—2 дня. Более достоверные данные дает измерение колебаний относительной плотности мочи в течение суток, в частности проба Зимницкого, которая состоит в оценке относительной плотности каждой из 8 трехчасовых порций мочи, собранных при произвольном мочеиспускании. Снижение максимальной относительной плотности мочи в пробе Зимницкого до 1012 и менее (гипостенурия) или ограничение колебаний относительной плотности мочи в пределах 1008—1010 (изостенурия, т.е. равенство относительной плотности мочи и относительной плотности безбелкового фильтрата плазмы) свидетельствует о выраженном нарушении концентрационной функции почек. Помимо колебаний относительной плотности мочи в пробе Зимницкого определяют соотношение дневного и ночного диуреза. У здорового человека дневной диурез значительно преобладает над ночным и составляет около 2/3—3/4 суточного диуреза. Более точно осморегулирующую функцию почек оценивают по осмоляльности сыворотки крови и осмоляльности мочи с вычислением концентрационного коэффициента (отношения осмоляльности мочи к осмоляльности сыворотки) и осмолярного клиренса.
Способность почек к регуляции кислотно-основного состояния устанавливают на основании определения рН мочи, титруемой кислотности мочи, экскреции бикарбонатов, аммиака и подсчета аммонийного коэффициента (отношения экскреции аммиака к общей секреции водородных ионов).
Исследование экскреции с мочой отдельных веществ (аминокислот, глюкозы, фосфатов и др.) позволяет обнаружить парциальные нарушения функции почек , что особенно важно для диагностики тубулопатий.
Практическое значение имеет также количественная оценка экскреции мочевой и щавелевой кислот. Обе кислоты фильтруются в почечных клубочках. Предполагается, что мочевая кислота подвергается почти полной реабсорбции, а увеличение ее экскреции (норма 400—600 мг в сутки) связано с усилением секреции. Снижение секреции с повышением уровня мочевой кислоты в крови (гиперурикемия) может быть следствием почечной недостаточности при заболеваниях почек и наблюдается также при использовании мочегонных средств тиазидового ряда, бутадиена и некоторых других препаратов, при ацидозе, дегидратации, застойной сердечной недостаточности.
Биопсия почки применяется для уточнения диагноза и оценки прогноза болезни. Чаще проводится чрескожная пункционная биопсия специальной иглой, реже — полуоткрытая биопсия. Чтобы морфологическая оценка изменений в почках была достаточно информативной, необходимо наличие в биоптате не менее 5—6 клубочков. Биоптаты исследуют с помощью светооптической микроскопии. Для определения типа нефрита и его активности дополнительно используют методы иммуногистохимического и электронно-микроскопического исследований. Биопсия почки особенно важна в тех случаях, когда решается вопрос о проведении активной терапии большими дозами глюкокортикоидов, цитостатиков, гепарином, а также плазмафереза. Абсолютно противопоказана биопсия почки при нарушениях свертывания крови, единственной функционирующей почке, сморщенных почках, неспособности больного вступать в контакт, тяжелой артериальной гипертензии. Относительными противопоказаниями к биопсии являются поликистоз почек, миеломная болезнь; поражение сосудов почек, способствующее кровоточивости (диабетический гломерулосклероз, узелковый периартериит).
Семиотика заболеваний почек включает как неспецифические симптомы (например, жалобы на боли в поясничной области, никтурию), так и характерные для определенных болезней почек специфические симптомы, синдромы и симптомокомплексы, обозначаемые в нефрологической практике как синдромы. Принято выделять так называемый мочевой и гипертензивный синдромы, нефротический синдром, остронефритический синдром, синдромы канальцевых дисфункций, а также синдромы острой и хронической почечной недостаточности. Некоторые синдромы (нефротический, гипертензивный) отличаются яркой клинической картиной с многочисленными проявлениями заболевания, для распознавания других синдромов необходимо использовать специальные методы исследований. Мочевой и гипертензивный синдромы могут быть следствием как двустороннего, так и одностороннего поражения почек. Мочевой синдром складывается из протеинурии, гематурии, лейкоцитурии и цилиндрурии.
Остронефритический синдром проявляется бурным возникновением или нарастанием отеков с типичной бледной одутловатостью лица, артериальной гипертензией (обычно диастолической), олигурией, протеинурией, гематурией, нередко нарушением функции почек. В ряде случаев клиника остронефритического синдрома дополняется его характерными осложнениями — почечной эклампсией, острой сердечной (левожелудочковой) недостаточностью, острой почечной недостаточностью. Возникновение остронефритического синдрома считается характерным для типичного начала острого гломерулонефрита (см. Нефриты).
Синдромы канальцевых дисфункций чаще наблюдаются у детей с наследственными тубулопатиями, реже у взрослых как поздно распознанный генетический либо как приобретенный дефект при заболеваниях почек с поражением их интерстиция или при внепочечных заболеваниях (опухоли, аутоиммунные болезни). Наиболее часто отмечается синдром почечного тубулярного ацидоза, который характеризуется сочетанием гиперхлоремического ацидоза с повышенной бикарбонатурией, высоким рН мочи и значительным снижением экскреции с мочой аммония и титруемых кислот. Тубулярная дисфункция (см. Тубулопатии) может проявляться также в форме почечной глюкозурии, фосфат-диабета (гипофосфатемический рахит), почечного несахарного диабета, синдрома Фанкони. Почечный гипертензивный синдром развивается практически при всех паренхиматозных заболеваниях почек, а также при поражении почечных сосудов (реноваскулярная артериальная гипертензия). Повышение АД при заболеваниях почек может быть обусловлено задержкой в организме натрия и воды с формированием объемзависимой гипертензии, активацией прессорной ангиотензин-альдостероновой системы и снижением депрессорной функции почек, обеспечиваемой синтезом простагландинов и конечных продуктов калликреин-кининовой системы — брадикинина и каллидина. Клинические проявления гипертензивного синдрома при болезнях почек определяются степенью повышения АД, поражением сердца и сосудов. Характерны жалобы на головную боль, ухудшение зрения, боли в области сердца, одышку. Так называемый синдром злокачественной почечной гипертензии проявляется значительным и стойким повышением диастолического АД, выраженной ретинопатией (с очагами геморрагий, отеком соска зрительного нерва, снижением зрения вплоть до полной слепоты), энцефалопатией, сердечной недостаточностью.
Важным признаком ряда заболеваний почек являются отеки, которые при нефротическом синдроме обусловлены гипопротеинемией со снижением онкотического давления плазмы, а при остром нефрите возникают в связи с повышенной сосудистой проницаемостью. Степень отеков варьирует от пастозности кожи лица, стоп до анасарки с асцитом, гидротораксом, гидроперикардом. Небольшая по степени задержка натрия и воды может не проявляться видимыми отеками; в таком случае ее определяют по увеличению массы тела больного на фоне снижения диуреза.
Симптомы функциональной недостаточности почек — см. Почечная недостаточность.
В современной классификации болезней почек выделяют следующие основные формы патологии: 1) врожденные аномалии количества, расположения и строения почек (пороки развития); 2) генетические нефропатии (тубулопатии); 3) инфекции, инвазии почек; 4) иммуновоспалительные заболевания почек (нефриты): а) первичные, б) вторичные, развивающиеся при системной красной волчанке, узелковом периартериите, гранулематозе Вегенера, болезни Гудпасчера, системной склеродермии, геморрагическом васкулите и др.; 5) нефропатии, обусловленные воздействием экзогенных химических, физических факторов (в т.ч. профессиональных); 6) поражения почек при метаболических, электролитных нарушениях; 7) амилоидоз почек; 8) нефролитиаз; 9) опухоли почек; 10) другие болезни почек. Последняя группа включает нефроптоз, вторичные поражения почек при аномалии их расположения и нарушениях оттока мочи (обструктивные уропатии), в частности гидронефроз, при венозном застое в почках и т.д. Из них одним из наиболее часто встречаемых, особенно у женщин, является нефроптоз (опущенная блуждающая почка) — патологическая подвижность почки, чаще правой, превышающая один позвонок при перемене положения тела из горизонтального в вертикальное.
При патологической подвижности почки могут возникнуть значительные гемо- и уродинамические нарушения, в частности венозная гипертензия в опущенной почке, перегибы мочеточника с затруднением оттока мочи, что может стать причиной развития пиелонефрита, гидронефроза, форникального кровотечения, нефролитиаза.
Основным симптомом неосложненного нефроптоза являются боли, иногда носящие характер почечной колики. Они обычно возникают в вертикальном положении больного и при физической нагрузке, стихают в горизонтальном положении, иногда сопровождаются ознобом, повышением температуры тела. Могут наблюдаться нарушения функции кишечника, психическая депрессия. Обычно удается прощупать подвижную почку, особенно в вертикальном положении больного. В моче могут определяться белок, эритроциты, лейкоциты, цилиндры. При экскреторной урографии, выполненной в горизонтальном и вертикальном положениях больного, видны избыточная подвижность почки и нарушение пассажа контрастной жидкости. В случае нефроптоза, осложненного артериальной гипертензией, производят аортографию и венографию при вертикальном положении больного. Двусторонний нефроптоз может быть одним из проявлений спланхноптоза, для диагностики которого необходима рентгеноскопия желудка.
Консервативное лечение нефроптоза состоит в ношении индивидуально изготовленного бандажа, который надевают утром в положении лежа и на выдохе. Рекомендуются специальный комплекс гимнастических упражнений для укрепления мышц передней брюшной стенки, плавание. Оперативное лечение показано при болях, лишающих трудоспособности, а также при осложнениях нефроптоза. Цель операции — нормализация уро- и гемодинамики фиксацией почки в ее физиологическом положении (нефропексия).
Нарушение развития почек в процессе эмбриогенеза выражается различными аномалиями их расположения (дистопии), взаимоотношения, формы, количества, аномалиями почечной паренхимы, чашечно-лоханочной системы и сосудов почек.
Аномалии расположения проявляются гомолатеральной (торакальной, поясничной, подвздошной и тазовой) или гетеролатеральной (перекрестной) дистопией почки . При торакальной дистопии почка обычно входит в состав диафрагмальной грыжи (см. Диафрагма). Мочеточник при этом удлинен, почечная артерия отходит от грудной части аорты. При поясничной дистопии почечная лоханка несколько повернута кпереди и находится на уровне IV поясничного позвонка; почечная артерия отходит аорты выше ее бифуркации. Подвздошная дистопия П. характеризуется более выражены ротацией почечной лоханки кпереди и расположением ее на уровне V поясничного — I крестцового позвонков. Почечные артерии, как правило, множественные, отходят от общей подвздошной артерии или от брюшной части аорты на уровне ее бифуркации. При тазовой дистопии П. располагается по средней линии позади и несколько выше мочевого пузыря, она, как правило, в той или иной степени гипоплазирована и имеет овальную, круглую или квадратную форму. Сосуды рассыпного типа являются ветвями общей подвздошной или внутренней подвздошной артерий. Гетеролатеральная (перекрестная) дистопия характеризуется смещением почки на противоположную сторону.
Дистопированная П. часто имеет дольчатое строение и обычно рассыпной тип кровоснабжения с короткими сосудами, ограничивающими ее смещаемость.
В клинической картине, обусловленной аномальным расположением органа, ведущим симптомом является боль, возникающая при перемене положения тела, физическом напряжении, метеоризме. При гетеролатеральной (перекрестной) дистопии боль обычно локализуется в подвздошной области и иррадиирует в паховую область на противоположной стороне. При торакальной дистопии почки клинические проявления и данные рентгенологического исследования могут напоминать опухоль средостения. При поясничной и подвздошной дистопии П. пальпируете виде слабоболезненного малоподвижного образования.
Диагноз устанавливают с помощью экскреторной урографии, а в случае резкого снижен функции П. — ретроградной пиелографии.
Лечение преимущественно консервативное. Оперативное лечение показано при дистопии осложненной гидронефрозом или почечно-каменной болезнью (см. Мочекаменная болезнь), гнойным пиелонефритом.
Аномалии взаимоотношения и формы (сращенные почки) подразделяют на симметричные (подковообразная и галетообразная почки), асимметричные (S-, L- и I-образные почки) формы сращения.
Симметричные формы сращения в виде подковообразной почки встречаются в 21/2 раза чаще у мальчиков. Форма подковы образуется при сращении П. нижними (90%) или верхними (10%) полюсами; на месте соединения П. имеется перешеек, образованный соединительной тканью или почечной паренхимой.
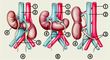
Основным клиническим признаком подковообразной почки является симптом Мартынова — Ровсинга — возникновение болей при разгибании туловища, связанное со сдавленном сосудов аортального сплетения перешейком П. Подковообразную П. иногда можно выявить при глубокой пальпации живота как плотное малоподвижное образование. Рентгенологически такая П. имеет вид подковы, выпуклая часть рой обращена чаще вниз (рис. 4), реже вверх. Наиболее четко контуры подковообразной почки определяются при экскреторной урографии и динамической сцинтиграфии, а также при компьютерной томографии.
Операции при подковообразной П. обычно производят в случае развития осложнений (гидронефроз, опухоль и др.). С целью выявлен характера кровоснабжения перед оперативным вмешательством показано проведение почечной ангиографии.
Галетообразная П. имеет вид плоскоовального образования, расположенного на уровне или ниже промонтория. У женщин она препятствует естественному процессу родов.
Диагноз основывается на данных пальпации пальцевого ректального обследования, а также результатах экскреторной урографии и абдоминальной аортографии. Поводом для оперативного вмешательства могут стать гнойный пиелонефрит, камни, туберкулез. Известны случаи удаления галетообразной почки, ошибочно принятой за опухоль.
Асимметричные формы сращения характеризуются соединением почек противоположными полюсами (рис. 5). Продольные оси почек сросшихся в виде латинских букв S и I, параллельны, а при L-образной почке — перпендикулярны друг другу.
Диагноз устанавливают при экскреторной урографии и сканировании П. При необходимости оперативного лечения (удаление камней, пластика по поводу уростаза и др.) показано проведение почечной ангиографии.
Аномалии количества наиболее часто встречаются в форме удвоения почек, в 2 раза чаще у девочек. Удвоение почек бывает полным и неполным. Для полного удвоения характерно наличие двух собирательных систем П. , каждая из которых имеет изолированное кровоснабжение. При неполном удвоении почек кровоснабжение ее обеих половин осуществляется одним сосудистым пучком. Мочеточники, отходящие от почечных лоханок удвоенной П. , впадают в мочевой пузырь раздельно либо сливаются в один ствол. Паренхима удвоенной П. имеет признаки гипоплазии, дисплазии. что способствует развитию различных заболеваний, в первую очередь пиелонефрита.
Аномалия диагностируется обычно при обследовании по поводу развивающихся осложнений. На экскреторных урограммах верхняя часть удвоенной почки может иметь признаки структурного и функционального недоразвития паренхимы и чашечно-лоханочной системы с более низким впадением устья мочеточника. При полной анатомической и функциональной неполноценности одной или обеих добавочных П. производят их удаление.
Аномалии почечной паренхимы включают агенезию, аплазию, гипоплазию и кистозные аномалии, а также наличие добавочной почки.
Агенезия почки — результат отсутствия закладки органа в процессе эмбриогенеза. Двусторонняя агенезия почек (арения) отмечается в 4 раза реже односторонней и преимущественно у плодов мужского пола. Дети с двусторонней агенезией П. обычно рождаются мертвыми, с множественными сочетанными пороками развития. При односторонней агенезии почек , как правило, отсутствуют соответствующие мочеточник и половая железа. Единственная П. обычно гипертрофирована и полноценна в функциональном отношении Подозрение на агенезию почек возникает при пальпации увеличенной безболезненной П. Диагноз устанавливают с помощью специальных исследований: при урографии на стороне агенезии почки отсутствует выделение контрастного вещества, с помощью цистоскопии выявляется наличие лишь одного мочеточникового устья; аортография указывает на отсутствие почечной артерии.
Аплазия почки — тяжелая степень недоразвития почечной паренхимы, нередко сочетающаяся с отсутствием мочеточника. П. представлена фибролипоматозной тканью, иногда с небольшим количеством функционирующих нефронов.
Обычно аплазия почки не проявляется клинически и распознается при обследовании по поводу заболеваний противоположной почки. Некоторые больные предъявляют жалобы на боли в боку или животе, что связано со сдавлением нервных окончаний фиброзной тканью и увеличивающимися кистами. В редких случаях отмечается артериальная гипертензия. На обзорной рентгенограмме в области аплазированной П. иногда обнаруживают кисты с обызвествленными стенками. При аортографии в этих случаях почечная артерия обычно не выявляется.
Необходимость лечебных мероприятий при аплазии почки возникает при резко выраженных болях, развитии гипертензии и рефлюксе в гипоплазированный мочеточник. Лечение оперативное — удаление аплазированной П. и мочеточника.
Гипоплазированная почка макроскопически выглядит как уменьшенный в размерах нормально сформированный орган. Гистологически имеются изменения, позволяющие выделить простую гипоплазию, гипоплазию с олигонефронией и гипоплазию с дисплазией. Простая гипоплазия характеризуется лишь уменьшением числа почечных чашечек и нефронов. При гипоплазии с олигонефронией уменьшение количества почечных клубочков сочетается с увеличением их диаметра, фиброзом интерстициальной ткани, расширением почечных канальцев. Гипоплазия с дисплазией сопровождается развитием соединительнотканных или мышечных муфт вокруг почечных канальцев, наличием клубочковых или канальцевых кист, а также включений лимфоидной, хрящевой и костной тканей.
Односторонняя гипоплазия П. клинически может быть бессимптомной. Однако в гипоплазированной П. нередко возникает пиелонефрит, зачастую приводящий к развитию нефрогенной гипертензии. Тяжелая форма двусторонней гипоплазии почек проявляется рано — в первые годы или даже недели жизни ребенка. Дети отстают в физическом развитии. Нередко наблюдаются бледность, рвота, понос, повышение температуры тела, признаки рахита. Отмечается выраженное снижение концентрационной функции П. Большинство детей с выраженной двусторонней гипоплазией почек погибает в первые годы жизни от уремии.
Одностороннюю гипоплазию обычно выявляют при рентгенологическом исследовании, предпринятом по поводу пиелонефрита. На экскреторных урограммах отмечается уменьшение размеров П. с хорошо контрастированной чашечно-лоханочной системой. Контуры почки могут быть неровными, число чашечек меньше, чем в норме, объем их уменьшен. Противоположная П. компенсаторно гипертрофирована. Большую помощь в дифференциальной диагностике оказывают ангиография и биопсия почек.
Лечение при односторонней гипоплазии, осложненной пиелонефритом и гипертензией, обычно сводится к нефрэктомии. При двусторонней гипоплазии почек , осложненной тяжелой почечной недостаточностью, может быть проведена двусторонняя нефрэктомия с последующей трансплантацией почки.
Добавочная (третья) почка — редкая аномалия, приобретающая клиническое значение при шеечной или внепузырной эктопии устья мочеточника с постоянным недержанием мочи либо при поражении добавочной почки воспалительным или опухолевым процессом. Добавочная П. обычно располагается ниже основной, имеет значительно меньшие размеры и собственное кровоснабжение за счет сосудов, отходящих непосредственно от аорты. Мочеточник впадает в мочевой пузырь самостоятельно либо сообщается с мочеточником основной П. Диагноз устанавливают на основании данных экскреторной урографии, ретроградной пиелографии, аортографии. Лечение (при необходимости) заключается в нефрэктомии добавочной почки.
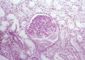
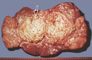
Кистозные аномалии паренхимы представлены различными по локализации и количеству кист вариантами (рис. 6). Среди них самый частый — поликистоз (рис. 6, а; рис. 7), или поликистозная дисплазия почек, поликистозная дегенерация, поликистозная болезнь, поражающая обе почки. Нередко сочетается с кистозными изменениями других органов, например печени, селезенки, реже легких, поджелудочной железы. Поликистоз почек , встречающийся у взрослых, передается доминантно с аутосомным и мономерным геном, а так называемый злокачественный поликистоз детского возраста — рецессивно. Кисты разделяют на гломерулярные, тубулярные и экскреторные. Гломерулярные кисты не имеют связи с почечными канальцами, приводят к раннему развитию почечной недостаточности. Тубулярные кисты образуются из извитых почечных канальцев, а экскреторные — из собирательных почечных трубочек. В раннем детском возрасте кисты мелкие, расположены как в мозговом, так и корковом веществе. Между ними определяется паренхима без диспластических изменений. У детей старшего возраста и взрослых П. значительно увеличены, деформированы за счет многочисленных кист различной величины. Островки паренхимы сдавлены кистами, нередко отмечаются изменения типа интерстициального нефрита. При поликистозе П. часто развиваются пиелонефрит, почечнокаменная болезнь, туберкулез почек.
Клинические проявления поликистоза почек неспецифичны. Возможны тупые боли в пояснице, периодическая гематурия, артериальная гипертензия, полиурия, гипоизостенурия и никтурия. При пальпации выявляются увеличенные бугристые П. Течение различается в разных возрастных группах. Чем раньше появляются клинические симптомы заболевания, тем злокачественнее оно протекает. У детей раннего возраста поликистоз почек нередко осложняется пиелонефритом, быстро приводящим к уремии. Присоединение пиелонефрита характеризуется соответствующими клиническими проявлениями, изменениями в анализах крови и мочи и прогрессирующим развитием почечной недостаточности.
Диагноз устанавливают с помощью экскреторной урографии, радиоизотопного и ультразвукового исследования и почечной ангиографии. На урограммах при сохраненной функции определяются увеличенные П. , удлинение и раздвигание шеек почечных чашечек с их колбовидной деформацией. На ранних стадиях процесса урографическая картина может быть не показательной. При радиоизотопном исследовании выявляют увеличение П. и дефекты паренхимы в связи с неравномерным накоплением радионуклида. Ангиографически определяются истончение и обеднение сосудистой сети, раздвигание артериальных ветвей.
Лечение направлено на борьбу с пиелонефритом, гипертензией, нарушениями водно-электролитного баланса. Часто оперативное вмешательство при поликистозе почек значительно утяжеляет состояние больного. Тем не менее оно становится необходимым при профузном почечном кровотечении, обтурирующем камне, нагноении кист, пионефрозе развитии злокачественной опухоли почек.
Прогноз при поликистозе почек чаще неблагоприятный. Больные редко живут более 10—12 лет после появления клинических симптомов, хотя известны случаи продолжительности жизни до 70 лет при доброкачественном течении заболевания.
Мультикистозная дисплазия (рис. 6, б) — аномалия, при которой обычно одна или, значительно реже, обе П. замещены кистами и полностью лишены паренхимы. Мочеточник при этом отсутствует или является рудиментарным. Двусторонняя мультикистозная дисплазия почек несовместима с жизнью. При одностороннем поражении клинические симптомы возникают в связи со сдавлением кистами окружающих органов. В этих случаях прибегают к нефрэктомии.
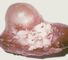
Солитарная киста (рис. 6, в) — одиночное кистозное образование, исходящее из паренхимы П. и выступающее над ее поверхностью. Диаметр кисты, как правило, не превышает 10 см. Киста обычно содержит серозную, изредка геморрагическую (вследствие кровоизлияния) жидкость. Редко встречается в почках дермоидная киста (см. Дермоид). Наиболее характерными клиническими признаками солитарной кисты П. являются тупая боль в области почек , пальпируемая опухоль и транзиторная гематурия. На обзорном снимке при расположении кисты на поверхности П. видна тень округлого образования, связанного с почкой. При расположении в паренхиме наблюдается выпячивание контура почки . При центральной локализации кисты отмечается диффузное увеличение органа. Решающее значение в диагностике кист принадлежит ультразвуковым и контрастным методам исследования. При экскреторной урографии устанавливают деформацию чашечно-лоханочной системы, при нефротомографии киста выявляется как округлый, четко очерченный участок просветления. На артериограмма зоне кисты имеется бессосудистый участок с раздвинутыми и огибающими его тонкими вытянутыми веточками сосудов (рис. 8). В нефрографической фазе в проекции кисты виден четко отграниченный дефект наполнения. В дифференциальной диагностике опухолей и кист помогает кистография (чрескожная пункция кисты с наполнением ее полости контрастным веществом).
Лечение оперативное. Если позволяет локализация кисты, то проводят ее вылущивают или вскрывают и тампонируют ее полость околопочечной клетчаткой. Пункция солитарной кисты с последующим наполнением ее склерозирующим раствором в половине случаев приводит к выздоровлению.
Мультилокулярная киста (рис. 6, г) — очень редкая аномалия, характеризующаяся замещением участка П. многокамерной, не сообщающейся с почечной лоханкой кистой. Остальная часть паренхимы не изменена и нормально функционирует. При росте кисты ее удается пальпировать через переднюю брюшную стенку. На урограммах отмечается дефект паренхимы с оттеснением или раздвиганием почечных чашечек, на ангиограммах он выглядит бессосудистым. Необходимость в лечебных мероприятиях возникает при развитии осложнений, например пиелонефрита. Лечение заключается в сегментарной резекции почки или нефрэктомии.
Губчатая почка (медуллярная кистозная почка, почка с губчатыми пирамидами) довольно редкая наследственная аномалия, которой кистозно расширены собиратель почечные трубки (рис. 6, д). Почки увеличены, на их поверхности имеются множествен кисты диаметром 1—2 мм. Клинически обычно отмечаются полиурия, изостенурия, приступы почечной колики (вследствие частого образования и отхождения конкрементов), пиелонефрит, возможны артериальная гипертензия, хроническая почечная недостаточность.
Диагноз устанавливают при обзорной и экскреторной урографии по типичному расположению в области почечных пирамид мелких теней мочевых камней и наличию гроздевидного расширения собирательных почечных бок. Лечение проводится лишь в случае развития осложнений.
Аномалии чашечно-лоханочной системы представлены, в основном, дисплазией почечных чашечек, сопровождающейся их врожденным увеличением (мегакаликоз), дистопией дивертикулом чашечек, гидронефрозом.
Мегакаликоз сопровождается недоразвитием почечных пирамид, уплощением почечных сосочков, в связи с чем малые почечные чашечки имеют округлую форму и увеличены в объеме. Обычно поражаются чашечки почки , реже только некоторые. Крайне редко встречается двусторонний мегакаликоз. Застой мочи в расширенных малых почечных чашечках способствует образованию камней и развитию пиелонефрита. На экскреторных урограммах отмечается значительное увеличение объема, а иногда и количества малых почечных чашечек, имеющих округлую форму. При этом лоханка не изменена, мочеточник свободно проходим для контрастного вещества.
Лечение консервативное, направлена борьбу с пиелонефритом. При образовании камней производят их удаление, иногда с резекцией полюса почки.
Чашечковый дивертикул (рис. 6, е) — аномалия, характеризующаяся наличием кистозного образования, связанного с малой почечной чашечкой узким каналом. Обычно чашечковый дивертикул отходит от верхней группы малых почечных чашечек (в 2 раза чаще справа, чем слева). Застой мочи в чашечковом дивертикуле нередко ведет к развитию пиелонефрита и образованию камней. Симптомами этих осложнений и проявляется клиническая картина чашечкового дивертикула.
Диагностика основана на данных экскреторной урографии. В сомнительных случаях выполняют ретроградную пиелографию, позволяющую четко видеть полость кисты и узкий ход, через который она сообщается с почечной чашечкой. Наиболее радикальным способом лечения служит удаление дивертикула с резекцией участка почки . Прогноз при оперативном лечении чаще благоприятный.
Аномалии почечных сосудов разделяют на аномалии артерий, вен и артериовенозные свищи.
Агенезия, аплазия и гипоплазия почечной артерии сопровождают соответствующие аномалии почечной паренхимы. Диагноз устанавливают с помощью почечной артериографии. На артериограмах гипоплазированная почечная артерия представляется укороченной и суженной на всем протяжении, что отличает ее от изображения почечной артерии при вторичном сморщивании почек.
Добавочные (аберрантные) почечные артерии встречаются довольно часто, но лишь в некоторых случаях они сопровождаются патологическими изменениями почечной паренхимы. Добавочные почечные артерии имеют меньший диаметр просвета, чем основной ствол сосуда. Отходя от аорты, добавочная точечная артерия направляется к нижнему или реже верхнему полюсу почки . Она может сдавливать мочеточник, вызывая нарушение оттока мочи. Диагноз устанавливают при сопоставлении экскреторных урограмм и почечных ангиограмм. Пересечение добавочной почечной артерии при оперативном вмешательстве может привести к развитию сегментарного некроза почки.
Двойная почечная артерия — два равноценных ствола почечной артерии, примерно одинакового калибра. Аномалия приобретает клиническое значение при операциях на почках , особенно при трансплантации почки.
Множественные почечные артерии кровоснабжают обычно подковообразную или дистопированную П. Их число и калибр широко варьируют, что может создавать большие трудности при операциях, поэтому перед вмешательством на дистопированной П. обычно проводят ангиографию.
Врожденный стеноз почечной артерии — концентрическое сужение артерии, приводящее к ухудшению трофики почки и развитию вазоренальной гипертензии. Чаще локализуется вблизи устья почечной артерии, но может располагаться на любом ее участке. Диагноз основан на данных артериографии и раздельном определении содержания ренина в оттекающей от почки крови. Лечение состоит в резекции суженного участка артерии или в ее протезировании. При значительных изменениях почки в случаях с выраженной гипертензией прибегают к нефрэктомии.
Врожденная аневризма почечной артерии наблюдается крайне редко. Ее клинические проявления, диагностика и лечение такие же, как при стенозе почечной артерии. Возможен спонтанный разрыв аневризмы с кровотечением в забрюшинное пространство и брюшную полость.
Фибромускулярная дисплазия — врожденное недоразвитие мышечной оболочки артерии с замещением ее фиброзной тканью — развивается преимущественно в средней трети почечной артерии, но может встречаться на всем ее протяжении. Иногда поражаются и добавочные почечные артерии. Клинические признаки в виде почечной гипертензии и гематурии появляются обычно в детском возрасте. Установлению диагноза помогают брюшная аортография и селективная почечная артериография. Лечение заключается в протезировании почечной артерии.
Кольцевидная почечная вена встречается только слева, что обусловлено ее более сложным, чем справа, эмбриогенезом и расположением. Кольцевидная вена представлена двумя ветвями: передняя проходит как обычно, задняя направляется косо вниз, обходит аорту сзади и впадает в нижнюю полую вену на уровне III—IV поясничных позвонков. Сдавление одного из стволов ведет к застойной почечной венозной гипертензии, что может проявиться альбуминурией, гематурией, варикозным расширением вен левого семенного канатика. Аномалия распознается с помощью венокавографии и селективной точечной венографии. В случаях выраженной венозной гипертензии прибегают к операции — наложению анастомоза между левой яичковой и общей подвздошной венами.
Ретроаортальная левая почечная вена отходит одним или реже несколькими стволами. Она идет косо вниз, проходит позади аорты и впадает в нижнюю полую вену на уровне II—IV поясничных позвонков. Клинические проявления, диагноз и лечебная тактика идентичны таковым при кольцевидной почечной вене.
Значительно реже наблюдается экстракавальное впадение левой почечной вены, чаще в левую общую подвздошную вену. Это затрудняет венозный отток крови от П. ввиду более высокого давления в общей подвздошной вене, чем в нижней полой. Диагноз основывается на данных венокавографии. Лечение такое же, как при кольцевидной почечной вене.
Врожденные артериовенозные свищи служат одной из причин венозной почечной гипертензии. Они могут локализоваться на любом участке сосудистого русла почки и распознаются с помощью селективной почечной ангиографии. Лечение: наложение ренокавального венозного анастомоза.
Различают закрытые (подкожные) и открытые (ранения) повреждения почек, которые могут быть изолированными или сочетаться с травмой других органов.
Закрытые повреждения разной тяжести (от незначительных кровоизлияний до полного размозжения почки) чаще бывают следствием непосредственной травмы поясничной области или сотрясения тела (например, при падении с высоты).
Выделяют пять основных групп закрытых повреждений почек (рис. 9): непроникающие разрывы почек, которые не достигают чашечек и лоханки, сопровождаются небольшой субкапсулярной гематомой без повреждения фиброзной капсулы (рис. 9, а); такие же непроникающие повреждения П. , но сопровождающиеся разрывом фиброзной капсулы с истечением крови в околопочечную клетчатку (рис. 9, б); проникающие повреждения с образованием глубоких трещин в паренхиме, разрывом свода одной из чашечек и истечением крови в лоханку без повреждения фиброзной капсулы почки (рис. 9, в) или сочетающиеся с разрывом капсулы и истечением крови и мочи в околопочечную клетчатку (рис. 9, г); размозжение П. — глубокие ее разрывы с отрывом сегментов, при этом в обширной урогематоме и имбибированной кровью жировой клетчатке располагаются свободные или висящие на сосудах куски органа (рис. 9, д). Помимо приведенных вариантов встречаются легкие повреждения почек (контузии) и реже — крайне тяжелые, характеризующиеся отрывом почек от сосудистой ножки, образованием большой гематомы в забрюшинном пространстве.
Клинические проявления закрытой травмы почек — гематурия, боли в поясничной области и ее припухлость при появлента гематомы, нарушение функции П. Ведущим признаком травмы почки является гематурия, интенсивность которой зависит от тяжести повреждения. Боль локализуется обычно в поясничной области, распространяется по ходу мочеточника. При прохождении сгустков крови по мочеточнику она приобретает характер почечной колики. Пальпация поясничной области резко болезненна, брюшная стенка и поясничные мышцы на стороне повреждения напряжены. При образовании забрюшинной гематомы могут отмечаться признаки раздражения брюшины.
Осложнения при закрытых повреждениях П. включают образование инфицированных урогематом, гнойное расплавление тромбов в сосудах почки и вторичное кровотечение. В этих случаях показаны срочная нефрэктомия и дренирование околопочечной клетчатки.
Диагноз устанавливают на основании анамнеза, клинической картины и данных рентгенологических исследований. На обзорном снимке мочевой системы выявляют сопутствующие повреждения скелета, отсутствие тени края поясничной мышцы на стороне повреждения при кровоизлиянии в околопочечную клетчатку, выраженную аэроколию на стороне травмы. Ценным рентгенологическим методом обследования при травме почек является экскреторная урография, которую производят после выведения больного из шока и стабилизации АД. С ее помощью определяют наличие у пострадавшего второй, нормально функционирующей почки и признаки сдавления чашечно-лоханочной системы поврежденной почки, затеки контрастного вещества в околопочечную клетчатку. Для более детального выявления локализации и степени повреждения чашечно-лоханочной системы проводят ретроградную пиелографию, которую целесообразно сочетать с хромоцистоскопией (см. Цистоскопия), позволяющей обнаружить выделение крови из устья мочеточника поврежденной почки. При возможности осуществляют ангиографию, позволяющую определить характер, масштабы, локализацию повреждения П. , сократить время обследования и на основании полученных результатов избрать наиболее рациональный метод и объем лечебных мероприятий. Ультразвуковое сканирование и компьютерная томография способствуют установлению травмы почек , однако по объему информации уступают почечной ангиографии.
Лечение в большей части случаев консервативное: больного обязательно госпитализируют, назначают строгий постельный режим на 2—3 нед., гемостатические средства и антибиотики. При значительной интенсивности и продолжительности внутреннего кровотечения, о котором судят по степени макрогематурии, величине поясничной гематомы, а также состоянию больного, необходима ревизия почек. По показаниям производят нефрэктомию или органосохраняющие операции — резекцию сегмента почки, ушивание разрыва паренхимы или лоханки. В этих случаях операцию обязательно сочетают с дренированием лоханки и околопочечного пространства.
Прогноз при закрытых повреждениях почек благоприятный. В ряде случаев наблюдаются сморщивание почек с появлением стойкой артериальной гипертензии, развитие посттравматического гидронефроза в результате рубцовых изменений в парауретральной клетчатке.
Открытые повреждения встречаются в виде огнестрельных, а также колотых и резаных ранений. Основными признаками открытого повреждения почек являются гематурия со сгустками, выделение крови и мочи из раны. Экскреторная урография обязательна и имеет те же достоинства, что и при закрытых повреждениях почек.
При открытом повреждении почек раненого экстренно госпитализируют; показаны раннее обнажение и ревизия почки после тщательного удаления сгустков крови, инородных тел, обрывков одежды и т.д. В случаях размозжения почки или разрыва паренхимы, проникающего в чашечно-лоханочную систему, повреждения магистральных сосудов производится нефрэктомия. При отрыве сегмента почки, касательных ранениях без глубоких разрывов почечной паренхимы показана органосохраняющая операция — ушивание раны. П. , дренирование лоханки и околопочечной клетчатки, что позволяет предупредить образование мочевой инфильтрации и гнойных затеков. Во всех случаях открытого повреждения почек назначают антибиотики широкого спектра действия.
Осложнениями при открытом повреждении П. являются анурия, которая может быть следствием ранения обеих почек или единственно функционирующей, возникновение паранефрита, уросепсиса, свищей.
По характеру ведущего патологического процесса большинство заболеваний почек , исключая опухоли, можно подразделить на две основные группы: воспалительные заболевания и заболевания, основой которых является дистрофия органа (многие из них обозначают как нефропатии), чаще всего обусловленная расстройствами кровоснабжения почек , нарушением обмена различных веществ в организме (метаболические нефропатии) либо токсическим повреждением нефронов (токсические нефропатии).
Расстройства кровоснабжения почек наблюдаются при сердечной и острой сосудистой недостаточности, при сужении просвета почечных сосудов, их закупорке тромбом, эмболом. При этом развивается гипоксическая дистрофия клеток нефронов, приводящая к повышению проницаемости клеточных мембран, нарушениям клубочковой и канальцевых функций ночек, а при тяжелых расстройствах почечной гемодинамики также к некрозу почечной ткани (см. Некроз почечных сосочков), формированию крупных инфарктов почек.
При сердечной недостаточности уменьшается почечный кровоток и развивается венозный застой в почках , что клинически проявляется снижением диуреза, никтурией, протеинурией, иногда микрогематурией. Выраженное этих симптомов пропорциональна степени сердечной недостаточности, при эффективном лечении они могут полностью исчезать. Острая сосудистая недостаточность (коллапс, шок) сопровождается анурией (из-за резкого снижения фильтрационного давления в клубочках в связи с падением АД), а при восстановлен диуреза после длительного коллапса в моче обнаруживаются в повышенных количествах белок, эритроциты, гиалиновые и клеточные цилиндры — следствие гипоксического повреждения нефронов. В большинстве случаев изменения мочи имеют преходящий характер. При гипертонической болезни признаки поражения почек характеризуют III стадию заболевания (или злокачественное течение болезни), когда формируется так называемая первично-сморщенная почка (см. Нефросклероз), характер периодическая или устойчивая протеинурия, микрогематурия, ретинопатия, постепенное развитие хронической почечной недостаточности. Дифференциальный диагноз с хроническим нефритом бывает очень трудным, т.к. основывается главным образом на анамнезе. Учитывают, что в отличие от проявлений хронического нефрита признаки первичного нефросклероза возникают обычно в более позднем возрасте, и через много лет после появления артериальной гипертензии отеки отсутствуют. Лечение только симптоматическое.
Стеноз почечной артерии (например, в связи с ее атеросклерозом, фибромускулярной дисплазией) клинически проявляется симптоматической артериальной гипертензией (см. Гипертензия артериальная), отличающейся особенно высокими значениями диастолического АД, нередко злокачественным течением и резистентностью к гипотензивной терапии, развитием ретинопатии. Предположить этот вид патологии помогают нередко выслушиваемый над стенозированной артерией систолический шум и значительная асимметрия изотопных ренограмм. Окончательно подтверждают диагноз с помощью почечной артериографии. Лечение хирургическое: выполняют реконструктивные операции с пластикой артерии: при атеросклеротическом стенозе производят чрезаортальную эндартериоэктомию, а также чрескожную транслюминальную баллонную дилатацию артерии.
Тромбоз и тромбоэмболия почечной артерии имеют сходные клинические проявления. Внезапно возникают резкие боли в поясничной области и животе, иногда рвота; повышается температура тела, нередко отмечается нейтрофильный лейкоцитоз, служит основанием подозревать острый живот. Предположить тромбоз почечных сосудов помогают снижение диуреза, появление гематурии, протсинурии при отсутствии объектив признаков перитонита. Подтверждают диагноз обнаружением частичного дефекта или полного отсутствия (при тотальном инфаркте органа) функции почек по данным экскреторной урографии, ренографии, динамической сцинтиграфии, с наибольшей достоверностью — результатами почечной артериографии: отмечается симптом «ампутации» ствола почечной артерии либо конусовидный бессосудистый участок в зоне инфаркта почки. Лечение — удаление тромба (эмбола) не позднее чем через 2 ч после появления первых симптомов тромбоза (эмболии); более позднее вмешательство может потребовать удаления почки. При мелких инфарктах почек назначают антикоагулянтную терапию.
Тромбоз почечной вены является, в основном, теми же симптомами, что и артериальный тромбоз, но венозный инфаркт почки протекает более тяжело, и при нем часто определяется увеличение почки, которая при пальпации напряжена и болезненна. Иногда выявляется расширение вен передней брюшной стенки и семенного канатика. Диагноз уточняют с помощью тех же исследований, что и артериальный тромбоз. Лечение состоит в раннем назначении антикоагулянтов и фибринолитических средств; при неэффективности тромболитической терапии производят тромбэктомию или нефрэктомию.
Метаболические нефропатии развиваются при генетически обусловленных или приобретенных нарушениях обмена различных веществ в организме. Из наследственных заболеваний, приводящих к развитию метаболических нефропатий, известны гликогенозы, оксалоз, первичная гиперуратурия и гиперурикемия (см. Подагра), цистиноз. Дисметаболическую природу имеет диабетическая нефропатия (см. Диабет сахарный). К распространенным причинам вторичных нефропатий относятся электролитные нарушения, особенно гипокалиемия и нарушения обмена кальция.
Оксалоз характеризуется избыточным образованием в организме щавелевой кислоты и сложением ее кристаллов в тканях внутренних органов. При этом в канальцах и в интерстициальной ткани почек откладываются кристаллы оксалата кальция (формируется нефрокальциноз), развиваются склеротические процессы в почках и почечная недостаточность. Диагностике помогает обнаружение устойчивой гипероксалурии, кристаллических оксалатов в моче. Лечение в основном заключается в назначении диеты: исключают из рациона продукты, богатые щавелевой кислотой (щавель, свеклу, какао, ревень и др.), назначают витамины В1 и В6, окись магния.
Гипокалиемия, сопровождающаяся обычно сочетанием внеклеточного алкалоза с клеточным ацидозом (в т.ч. в клетках канальцев П. ), рано проявляется ослаблением концентрационной способности почек, которое вначале связано с функциональными нарушениями реабсорбции натрия в канальцах. В последующем (при длительной гипокалиемии) развиваются процессы дистрофии клеток канальцев и склероз интерстиция, что приводит к стойкому нарушению концентрационной функции почек, полиурии и вторичной полидипсии. Эти симптомы и снижение осмотической плотности мочи у больных с гипокалиемией являются основой диагноза гипокалиемической нефропатий. Лечение — см. Гипокалиемия.
Нарушения обмена кальция сопровождаются усиленным его выведением через почки как при гиперкальциемии, так и вследствие вторичного гиперпаратиреоза при гипокальциемии. Избыточная нагрузка кальцием почечных канальцев приводит к их дистрофии (вначале преимущественно в дистальных отделах), что сопровождается снижением концентрационной функции почек. В последующем нарушение почечных функций усугубляется отложением кальция в просвете канальцев с их обструкцией, вовлечением в процесс клубочков интерстиция с развитием распространенного нефрокальциноза. Клинически этот вид нефропатии характеризуется значительной полиурией, полидипсией, выраженным снижением осмотической плотности мочи, что в ряде случаев требует дифференциальной диагностики с несахарным диабетом (см. Диабет несахарный). В отличие от последнего при нефрокальцинозе степень полиурии под влиянием питуитрина существенно не изменяется. Лечение направлено на основное заболевание, с которым связано крушение обмена кальция.
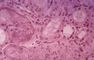
Токсические нефропатии наблюдаются при острых и хронических отравлениях различными ядами, выводимыми из организма через почки. При этом морфологически определяются разной степени дистрофические изменения эпителия канальцев, иногда с признаками вторичной воспалительной реакции (рис. 10). Очень тяжелые поражения почек , сопровождающиеся почечной недостаточностью, отмечаются при отравлении сулемой и некоторыми другими солями тяжелых металлов (см. Отравления, Отравления профессиональные). Особо выделяют лекарственные поражения почек, которые могут развиваться как по типу токсической нефропатий, так и в форме лекарственного нефрита, обусловленного патологической иммунной реакцией с отложением в почках циркулирующих иммунных комплексов (см. Нефриты, Побочные действия лекарственных средств).
Токсическое повреждение почек вызывают не все лекарственные средства, а лишь те из них, которые способны взаимодействовать с биохимическими субстратами и физиологическими процессами в клетках нефронов или интерстиция П. (взаимодействие с рецепторами, угнетение клеточного дыхания, процессов синтеза, блокада ферментов трансмембранного переноса катионов и т.д.). Возможность и характер такого взаимодействия определяют свойство и степень нефротоксичности лекарственного средства. При этом для ряда препаратов (например, бутадиона, салициловокислого натрия) вероятность развития лекарственной нефропатий пропорциональна в основном длительности их применения, но для большинства нефротоксичных средств она зависит от концентрации препарата в крови (следовательно, от его дозы), а также от возможности реабсорбции лекарственного средства в канальцах (для фильтрующихся в клубочках), определяющей степень проникновения его в интерстициальную ткань почек. Из широко применяемых медикаментов нефротоксичностью при передозировке обладают тиазидные диуретики, цитостатики, тубазид, сульфаниламиды, нитрофураны, многие антибиотики, в частности аминогликозиды (неомицин, канамицин, гентамицин, стрептомицин), полимиксины, амфотерицины, ристомицин, метациллин, цефалоридин.
В большинстве случаев лекарственные токсические нефропатий проявляются только изменениями мочи (протеинурия, микрогематурия, снижение осмотической плотности), иногда отмечаются полиурия, жажда. У больных с исходным нарушением выделительной функции почек применение нефротоксических лекарственных средств (даже в обычных терапевтических дозах) может привести к прогрессированию почечной недостаточности. При появлении признаков лекарственной нефропатий вызвавший ее препарат необходимо отменить. При заболеваниях почек назначения нефротоксических лекарственных средств следует избегать или применять их в тем меньших дозах, чем больше нарушена выделительная функция почек.
Смещающий липоматоз — разрастание жировой ткани в забрюшинном пространстве вокруг почки. В процесс вовлекаются также соседние органы и ткани. Клинически заболевание проявляется болью, наличием опухолевидного образования, диспепсией. Диагноз устанавливается с помощью рентгеноурологических методов исследования, выявляющих деформацию чашечно-лоханочной системы и смещение почки. Дифференциальный диагноз проводят с гидронефрозом, опухолью почки, кистой яичника, кистой поджелудочной железы, спленомегалией.
Лечение оперативное — полное удаление липоматозных масс; в случае прорастания ими почки производят нефрэктомию.
Воспалительные заболевания почек могут быть неинфекционными и инфекционными, по течению — острыми и хроническими. Из неинфекционных воспалительных заболеваний основную группу составляют первичные и вторичные нефриты иммунного генеза (см. Нефриты). Инфекционные поражения почек по этиологии подразделяют на специфические, к которым относят, например, сифилис почек, туберкулез почек (см. Туберкулез внелегочный, туберкулез мочевых органов), и неспецифические — пиелонефрит, карбункул, гангрена почки, поражение почки при сепсисе, подостром бактериальном эндокардите (см. Эндокардит), септицемии при различных бактериальных инфекциях. К редким относятся грибковые заболевания почки , в частности актиномикоз, кандидамикоз. Среди вирусных инфекций тяжелым поражением почек (нередко с развитием острой почечной недостаточности) характеризуется геморрагическая лихорадка с почечным синдромом. Отдельную группу составляют паразитарные заболевания почек.
Карбункул почки возникает при инфицировании в П. очагов некроза (инфарктов), подвергающихся при этом гнойному расплавлению в виде сливающихся между собой абсцессов, вокруг которых формируется плотный напряженный инфильтрат, сдавливающий почку, что нарушает уродинамику и кровоток в почечных сосудах. Возможен прорыв гноя в одну из почечных чашечек или через капсулу почки; в последнем случае развивается паранефрит, который, в свою очередь, может осложниться поддиафрагмальным абсцессом, гнойным плевритом, панкреатитом, перитонитом.
Общие клинические проявления соответствуют картине сепсиса: отмечаются вначале гектическая, затем постоянная лихорадка, повторные ознобы, потливость, симптомы общей интоксикации (тошнота, рвота, головная боль), увеличение селезенки, печени (через несколько дней), иногда развиваются инфекционно-токсический шок, острая почечная недостаточность. Возможны жалобы на боль в поясничной области (чаще справа в соответствии с более частой локализацией карбункула в правой почке), обычно иррадиирующую под лопатку, в подвздошную область, иногда в подреберье; учащенное и болезненное мочеиспускание; нередко наблюдается олигурия. Пальпация и суккуссия пораженной почки обычно резко болезненна. Определяются признаки пареза кишечника, напряжение мышц живота, спины. При наличии контрактуры большой поясничной мышцы или (и) воспалительной инфильтрации мягких тканей поясничной области следует предполагать паранефрит.
Диагноз устанавливают на основании характерной клинической картины и данных дополнительных исследований. Если отток мочи из пораженной почки не нарушен, то в мочевом осадке обнаруживаются эритроциты и в больших количествах лейкоциты и бактерии (при прорыве гноя в лоханку отмечается выраженная пиурия), но при блокированном оттоке изменения осадка мочи незначительны. В крови заявляют повышение СОЭ, гиперлейкоцитоз (в редких случаях лейкоцитопению), изменение содержания белков крови, характерное для острой фазы воспаления (появление С-реактивного протеина, увеличение содержания фракции a-глобулинов и др.) Локализацию и характер поражения почки устанавливают с помощью обзорной рентгенографии (могут быть обнаружены увеличение размеров и смещение пораженной почки, сколиоз, нечеткость контура большой поясничной мышцы), ультразвукового исследования почек , дискреторной урографии, ретроградной уретеропиелографии, ангиографии. При этом определяют выбухание контура почки, деформацию почечных чашечек, дефекты паренхимы в зоне инфильтрата, изменения сосудистого русла почки.
Лечение требует как можно более раннего дренирования пораженной почки, поэтому при предположительном диагнозе карбункула почки больного срочно госпитализируют. Проводят антибактериальную и интенсивную дезинтоксикационную терапию, при недостаточной эффективности которой производят декапсуляцию почки или применяют другие методы хирургического лечения вплоть до нефрэктомии. В случае развития острой почечной недостаточности осуществляют гемодиализ.
Гангрена почки — тяжелая форма гнойного пиелонефрита, вызванного возбудителями анаэробной инфекции (анаэробные кокки, клостридии и др.). Развивается при сочетанных повреждениях почки и кишечника, иногда при анаэробном сепсисе. Клинические проявления сходны с таковыми при карбункуле почки. Диагноз устанавливают на основании обнаружения при обзорной рентгенографии пузырьков газа в ткани П. и в околопочечной клетчатке. Принципы лечения те же, что при карбункуле почки, применяют нефрэктомию и широкое дренирование забрюшинного пространства.
Паразитарные заболевания почек. Эхинококкоз почек вызывается личинкой ленточного гельминта Echinococcus granulosus. Гидатида заносится в почку обычно током артериальной крови и развивается преимущественно в корковом веществе, образуя эхинококковую кисту. Левая почка поражается чаще. Инвазия происходит обычно в детстве, но из-за медленного роста киста выявляется чаще в возрасте 20—50 лет.
Различают закрытую кисту с неповрежденной стенкой (рис. 11), псевдозакрытую кисту, пролабирующую в почечную чашечку и омываемую мочой, и открытую кисту, сообщающуюся с чашечно-лоханочной системой, следствием чего может быть эхинококкурия. В зависимости от величины и расположения эхинококковой кисты происходят смещение почки, деформация и расширение почечных чашечек и лоханки, атрофия почечной паренхимы.
Клинические проявления эхинококкоза почки зависят от расположения и величины эхинококковой кисты, характера патологических изменений в почке, а также токсического действия паразита на организм (см. Эхинококкоз). В течении болезни различают латентный период (от момента внедрения паразита до появления первых клинических симптомов) и период клинических проявлений. Латентный период обычно имеет большую продолжительность (многие годы), что объясняется медленным ростом эхинококковой кисты. В этот период паразит может погибнуть и подвергнуться в дальнейшем обызвествлению. К ранним клиническим проявлениям относятся первые признаки интоксикации: легкое недомогание, быстрая утомляемость, слабость, снижение аппетита, потеря в весе. В последующем появляются более специфичные симптомы заболевания, относящиеся к периоду клинических проявлений: медленно растущее опухолевидное образование в подреберье, тупая постоянная боль в подреберье или поясничной области, почечная колика, субфебрильная (иногда фебрильная) температура, в некоторых случаях кожный зуд, эозинофилия крови. Отхождение с мочой дочерних эхинококковых пузырей обычно сопровождается почечной коликой, гематурией, а иногда обострением пиелонефрита, дизурией, задержкой мочи, при прорыве нагноившейся кисты — лейкоцитурией.
Диагноз заболевания устанавливается быстро лишь в редких случаях эхинококкурии, в остальных случаях он затруднен и может быть поставлен только в результате комплексного обследования. Имеют значение сведения о профессии больного, проживании в районах распространения гельминтоза, о контакте с домашними животными. Кисты нижнего сегмента почки пальпируются в виде округлых опухолевидных образований в подреберье. За счет воспаления и спаяния с окружающими тканями нарушается подвижность почки. Поверхность кисты гладкая или бугристая, консистенция ее плотная, реже эластичная. Симптом Пастернацкого бывает положительным при присоединении воспалительного процесса или нарушении оттока из ранее открытой кисты. Изменения мочи при закрытой форме эхинококкоза почки наблюдаются редко; возможны лейкоцитурия, гематурия, иногда (как следствие токсического действия эхинококка на почку) протеинурия, цилиндрурия. При открытой форме пиурия встречается в 60%, гематурия — в 20% случаев; моча мутная, содержит хлопья, обрывки некротизироваиной ткани. В крови примерно у 20% больных выявляется эозинофилия, примерно у трети больных — умеренный лейкоцитоз, у 65% — повышение СОЭ. Большое диагностическое значение имеют реакция латекс-агглютинации, реакция непрямой гемагглютинации, иммуноферментный анализ, которые, однако, при погибшем эхинококке бывают отрицательными.
При цистоскопии определяются неспецифические изменения слизистой оболочки мочевого пузыря, в редких случаях (при эхинококкурии) видны рождающиеся или свободно плавающие дочерние пузыри. С помощью обзорной рентгенографии мочевых путей могут быть обнаружены увеличение почки, обызвествление стенок кисты в виде нежной, едва заметной линии либо четкого кольцевидного образования. При гибели и обызвествлении дочерних пузырей киста выявляется в виде гомогенного или перистого округлого образования. помощью экскреторной урографии определяют изменения чашечно-лоханочной системы пораженной почки. Компьютерная томография позволяет установить плотность тканей и сред, что играет существенную роль в распознавании кисты и опухоли почки, локализацию и распространенность патологического процесса в органе. Ультразвуковое исследование почки также дает возможность получить представление о макроструктуре объемного образования, дифференцировать кисту с опухолью, однако характера кисты в большинстве наблюдений определить не удается. С помощью ангиографии при эхинококкозе почки выявляется бессосудистое образование. Сканирование почек и динамическая сцинтиграфия позволяют определить локализацию, объем и степень деструкции органа. Совокупность результатов перечисленных исследований является основой дифференциального диагноза эхинококкоза почки с опухолью, солитарной кистой, гидронефрозом, почечнокаменной болезнью.
Лечение оперативное: удаление паразитной кисты при максимальном сохранении функционирующей почечной ткани. Производят: эхинококкэктомию, резекцию почки, иногда, нефрэктомию.
Прогноз зависит от распространенности; эхинококкоза и от выраженности интоксикации организма. При разрыве эхинококкового пузыря с обсеменением полостей и тканей прогноз ухудшается.
Альвеококкоз почек вызывается паразитом Echinococcus alveolaris (multilocularis) в личиночной стадии и характеризуется образованием в почках очагов продуктивно-некротического воспаления с пролиферацией соединительной ткани в форме узла, который макроскопически выглядит как злокачественная опухоль, но в ткани узла определяются многочисленные мелкие спавшиеся пузырьки паразита. Встречается крайне редко. Во всех случаях, обнаружения альвеококкоза почки первичный очаг находился в печени, а почка вовлекалась в процесс вторично за счет инфильтративного роста по межтканевым щелям.
Диагноз и дифференциальный диагноз альвеококкоза П. с эхинококкозом почки затруднен, т.к. увеличение почки, повышение плотности, обызвествление, эозинофилия, положительная реакция латекс-агглютинации возможны при обоих заболеваниях. Гематурия, пальпируемое образование в почечной области позволяют заподозрить новообразование почки. При альвеококкозе рентгенологически проекции почки обнаруживают неясно очерченную тень, иногда участки перистого обызвествления, на экскреторных урограммах и ретроградной пиелограмме — оттеснение почечных чашечек и лоханки, их деформацию; при значительном поражении почки на урограмме отсутствует выделение контрастного вещества.
Лечение оперативное. Прогноз серьезный. Обычно больные погибают от печеночной недостаточности или кахексии, реже от метастазов альвеококкоза в головной мозг. См. также Альвеолярный эхинококкоз.
Филяриатозы возникают вследствие поражения личинками паразита (микрофилярий) при укусе некоторыми видами комаров; сопровождаются лимфогенным поражением почек. Первично поражается лимфатическая система — извиваются лимфангииты с тромбозом и склерозом лимфатических сосудов, расширением их коллатералей, лимфостазом, повышением гидростатического давления, приводящим к разрыву лимфатических сосудов и излиянию лимфы в мочевые пути. Клинически это проявляется хилурией, а при дополнительном разрыве кровеносных сосудов — гематохилурией.
Большинство больных отмечают тяжесть в поясничной области (чаще на стороне поражения), повторяющиеся приступы почечной колики. Возможны затрудненное мочеиспускание и даже задержка мочи Хилурия может быть постоянной или возникать периодически. Ее появление или усиление может быть спровоцировано приемом обильной жирной пищи, физической нагрузкой, беременностью. Моча при хилурии имеет белесоватый цвет за счет эмульгированных нейтральных жиров. Жир определяется в моче макроскопически или в виде мельчайших капель под микроскопом. При присоединении гематурии моча приобретает кровавый или бурый цвет Кроме жира, эритроцитов и лейкоцитов в моче содержатся белок и фибриноген, с чем связано образование сгустков. Они нарушают отток мочи из почечной лоханки, обусловливают боли ноющего характера в поясничной области или почечную колику; при наличии сгустков в мочевом пузыре отмечается затрудненное мочеиспускание или задержка мочи.
Диагноз устанавливают на основании обнаружения жира, белка в моче и микрофилярий в моче или крови Для выявления лимфоуринарного соустья производят прямую лимфангиоаденографию.
Лечение состоит в применении дитразина цитрата и оперативном разрушении лимфатических связей почки с основными лимфатическими коллекторами Прогноз при своевременном лечении благоприятный. См. также Филяриатозы.
Шистосомоз почек встречается крайне редко, имеются единичные наблюдения непосредственного поражения почки. Обычно почка вовлекается в процесс в связи с обструкцией мочеточника вследствие интрамурального отложения в нем яиц Schistosomf haematobium и вторичного продуктивно-склеротического процесса а его стенках, что приводит к гидронефрозу и способствует развитию хронического пиелонефрита.
Клинически отмечаются ноющие боли в поясничной области, приступы острых болей на стороне поражения, нередко признаки пиелонефрита.
Диагноз устанавливают на основании обнаружения яиц паразита в моче, выявления специфических изменений заболевания на слизистой оболочке мочевого пузыря при цистоскопии и типичных изменений на экскреторной урограмме — определяются колбовидное расширение мочеточника над стриктурой терминального отдела, гидронефроз.
Лечение оперативное (после предшествующей терапии антишистосомными средствами). В основном производят пластические операции на нижней трети мочеточника, направленные на восстановление пассажа мочи. При значительном поражении почки (выраженный гидроуретеронефроз) показана нефрэктомия. См. также Шистосомозы.
Аскаридоз почек встречается крайне редко, может быть связан с миграцией личинок по кровеносной системе либо с проникновением личинок и зрелых аскарид в околопочечную клетчатку и почку при перфорации стенки кишки. Влияние гельминтоза на почки может характеризоваться дистрофическими изменениями эпителия почечных канальцев, что клинически может проявляться протеинурией, микрогематурией, увеличением содержания в осадке мочи эпителиальных клеток. Лечение — см. Аскаридоз.
Трихинеллез почек мало изучен. Инвазия сопровождается протеинурией и эритроцитурией разной степени. По данным биопсии в почке развивается мезангиальный пролиферативный гломерулонефрит. Возможно возникновение вторичного пиелонефрита при внедрении трихинелл в мускулатуру органов мочевой системы См. также Трихинеллез.
Различают первичные доброкачественные и злокачественные опухоли почек и более редкие вторичные (метастатические) злокачественные новообразования почки, в частности при метастазах злокачественного карциноида (рис. 12).
Доброкачественные опухоли почек — аденома, миома, фиброма, лейомиома, липома, гемангиома, лимфангиома, хондрома, остеома, миксома, дермоид почки, папиллома и эндометриома лоханки — встречаются редко. Обнаруживаются они (чаще всего аденома) случайно либо при обследовании больного в связи с гематурией.
Доброкачественные опухоли П. могут малигнизироваться, поэтому диагностическая и лечебная тактика в основном такая же, как и при злокачественных опухолях. Во всех случаях необходимо комплексное обследование больного, причем экскреторная урография и ультразвуковое исследование могут быть выполнены в амбулаторных условиях. При подозрении на опухоль показана ревизия почки вплоть до срочного гистологического исследования. Если при этом будет доказан доброкачественный характер опухоли, то возможно выполнение органосохраняющей операции — энуклеации опухоли или резекции почки. Прогноз при доброкачественных опухолях почки благоприятный.
Злокачественные опухоли почек составляют 2—3% всех злокачественных новообразований и около 5% всех урологических заболеваний у взрослых. Наиболее распространенной злокачественной опухолью почечной паренхимы является аденокарцинома (см. Рак), редко встречаются саркома почки и раковые опухоли лоханки. У детей одной из самых частых опухолей почки является нефробластома (эмбриональная нефрома, аденосаркома) — дизонтогенетическая опухоль почки, обозначаемая иногда как опухоль Вильмса по имени описавшего ее немецкого хирурга (М. Wilms, 1899).
Аденокарцинома (гипернефроидный рак почки, гипарнефрома) одинаково часто локализуется в правой и левой П. , иногда (не более чем в 1,5% случаев) наблюдаются двусторонние опухоли. По гистологическому строению выделяют несколько вариантов опухоли: светлоклеточный, альвеолярный, зернисто-клеточный (темноклеточный), солидно-тубулярный, веретено-клеточный (полиморфный), саркомоподобный, железистый (тип обычной аденокарциномы). Светлоклеточный рак составляет большинство эпителиальных новообразований почки у взрослых. Опухоль состоит из одного или нескольких узлов округлой формы, на разрезе имеет пестрый вид с желтыми, коричневыми или красными вкраплениями (рис. 13). Ее характерный гистологический признак — наличие полигональных или кубических клеток со светлой («пустой») протоплазмой, образующих солидные, нередко также железистые структуры.
Саркома почки отличается быстрым ростом с частым прорастанием в почечные вены, ранним метастазированием в различные органы. Опухоль обычно больших размеров, бледно-серого цвета, мягкой или плотной консистенции (рис. 14).
Раковые опухоли почечной лоханки иногда сочетаются с такими же опухолями других отделов мочевых путей; нередко развитию опухоли предшествуют пиелонефрит, нефролитиаз.
Отмечают связь этих опухолей с длительным приемом фенацетина. Чаще всего встречается папиллярный рак лоханки (рис. 15).
Клиническая картина. Злокачественные опухоли почек чаще наблюдаются у мужчин (примерно в 2,5—3 раза чаще, чем у женщин) в возрасте после 40 лет. У разных больных и в разных стадиях опухолевого процесса картина заболевания может существенно различаться из-за различного соотношения общих и местных проявлений болезни и в зависимости от развития паранеопластических синдромов, наличия и локализации метастазов. Выделяют ренальные и экстраренальные (общие) симптомы опухоли.
К ренальным симптомам относят гематурию, боли, пальпируемую опухоль. Эта классическая триада встречается не всегда и характерна для далеко зашедшего процесса. Гематурия, как правило, тотальная, безболевая, интенсивная, иногда со сгустками крови в моче в виде «червячков», может продолжаться от нескольких часов до нескольких дней, внезапно возникает и так же прекращается. Иногда на высоте макрогематурии развивается типичный приступ почечной колики, связанный с окклюзией мочеточника сгустком крови, что может быть ошибочно интерпретировано как проявление мочекаменной болезни. Но в отличие от нее при опухоли почки гематурия появляется не после колики, а предшествует ей. Нередко опухоль почки сопровождается микрогематурией, связанной с кровотечением из форникальных вен. Боли при опухолях почки вследствие растяжения фиброзной капсулы носят тупой, ноющий характер, но они становятся мучительными при сдавлении или прорастании опухолью нервных стволов и поясничных корешков. Пальпируемая опухоль занимает третье по частоте место среди клинических проявлений. Чаще всего она исходит из нижнего полюса почки, плотная, бугристая и в зависимости от стадии процесса либо сопутствующего вторичного воспаления подвижная или совершенно неподвижная. Ценным для диагностики местным симптомом является варикоцеле, не исчезающее при перемене положения тела.
Общие симптомы, как и при злокачественных опухолях других органов, мало специфичны. Наряду с общей слабостью, недомоганием, кахексией (обычно на фоне анорексии) при злокачественных опухолях П. заслуживают внимания такие симптомы, как лихорадка, которая носит постоянный или интермиттирующий характер; эритроцитоз (вторичный) либо, напротив, анемия (вследствие интоксикации из-за распадающейся опухоли или длительной интенсивной гематурии), иногда артериальная гипертензия, исчезающая после удаления опухоли; повышение СОЭ. Паранеопластические синдромы чаще выражаются дерматозом, нейромиопатией, остеоартропатией. Они могут предшествовать типичной клинической картине или сопровождать ее.
При нефробластоме у детей нередко первым и ведущим симптомом бывает сама растущая опухоль, замечаемая родителями по увеличению живота ребенка. Не всегда наблюдаются сопутствующие боли в животе, снижение аппетита, тошнота, субфебрилитет.
У ряда больных первым проявлением рака почки являются метастазы в легкие, кости, регионарные или отдаленные лимфатические узлы. Метастазы в легкие на рентгенограммах имеют вид округлых шаровидных теней, одиночных или множественных. Для костных метастазов характерно поражение длинных трубчатых костей, таза, позвоночника, ребер. Они имеют остеолитический тип, могут быть причиной патологических переломов. При лимфогенном метастазировании в первую очередь поражаются паракавальные и параортальные лимфатические узлы, затем узлы средостения, шеи, паховые и подвздошные.
Диагноз злокачественной опухоли почки на ранней стадии ее развития затруднен из-за невыраженности местных и неспецифичности общих клинических проявлений. Аденокарциному почки следует предполагать при наличии у больного неясных по происхождению устойчивой лихорадки (особенно в сочетании с эритроцитозом или анемией), гематурии, повышения СОЭ. Во всех этих случаях необходимо целенаправленное урологическое обследование больного. В амбулаторных условиях важную диагностическую информацию могут дать экскреторная урография и ультразвуковая томография почек. Амбулаторно (в диагностическом центре) может быть произведена компьютерная томография почки , позволяющая установить наличие и оценить размеры опухоли (рис. 16). В условиях стационара проводят более углубленное обследование, осуществляя цитологическое исследования осадка мочи (иногда обнаруживаются атипичные клетки), сканирование, сцинтиграфию. П. , абдоминальную аортографию с селективной почечной артериографией, венокавографию с селективной почечной венографией, при опухолях лоханки также пиелографию, пиелоскопию. Селективная почечная ангиография имеет важное дифференциально-диагностическое значение, позволяя определять изменения сосудистого русла пораженной почки, характерные для опухоли (рис. 17) или свойственные другим объемным образованиям в почке (парапельвикальные и солитарные кисты, гидронефроз, карбункул почки).
Всестороннее обследование больного, включающее рентгенологические и другие исследования не только почек , но и легких, печени, костной и других систем, позволяет установить и сформулировать диагноз злокачественного новообразования почки в соответствии с требованиями к формулированию диагноза по системе TNM, предложенной Международным противораковым союзом в 1973 г. В этой системе экспансивный рост опухоли, поражение лимфатических узлов и наличие отдаленных метастазов характеризуются следующим образом:
Т1 — маленькая опухоль без увеличения размеров почки, имеются ограниченная дисторсия или деформация чашечки, деформация сосудов почечной паренхимы; Т2 — большая опухоль с деформацией и (или) увеличением чашечек либо лоханки (по данным аортографии целостность коркового слоя сохранена); Т3 — распространение опухоли на околопочечную, окололоханочную жировую клетчатку или сосудистую ножку почки; Т4 — распространение опухоли на соседние органы или брюшную стенку.
N0 — регионарные лимфатические узлы не поражены; N1 — поражение одного гомолатерального лимфатического узла; N2 — поражение контралатеральных или билатеральных лимфатических узлов или наличие множественных метастазов в регионарных лимфатических узлах; N3 — несмещаемые метастазы в регионарных лимфатических узлах (оцениваются только при хирургическом вмешательстве); N4 — поражение юкстарегионарных лимфатических узлов;
М0 — нет признаков отдаленных метастаз; М1 — имеются отдаленные метастазы.
В некоторых случаях правильный диагноз качественной опухоли почки и ее характеристика в символах TNM системы возможны только во время операции.
Лечение. Единственный радикальный метод лечения злокачественных опухолей почки — нефрэктомия. Она показана во случаях, когда операция технически возможна, здорова другая почка и нет противопоказаний общего порядка. Множественные метастазы в легкие при общем удовлетворительном состоянии не являются противопоказанием к операции. Солитарные метастазы в легкие и кости подлежат удалению через некоторое время после нефрэктомии или одновременно с ней. Лучевая терапия при раке почки применяется после нерадикально выполненной операции, а также с паллиативной целью (для снятия болей).
В неоперабельных случаях для борьбы с непрекращающейся гематурией прибегают к эмболизации почечной артерии. Химиотерапия не эффективна.
Прогноз при злокачественных опухолях почки неблагоприятный. Продолжительность жизни большинства неоперированных больных с момента появления первых симптомов составляет 1—3 года (известны лишь единичные случаи выживания до 5 и более лет). У оперированных больных 5-летняя выживаемость составляет не более 45%.
Большинство хирургических операций на почках производят при положении больного на боку в условиях общей анестезии с применением мышечных релаксантов и искусственной вентиляции легких. Чаще всего осуществляют внебрюшинный доступ к П. используя различные варианты вскрытия забрюшинного пространства (люмботомии). Наиболее распространенными операциями являются декапсуляция почки, нефро- и пиелостомия, нефротомия, резекция почки и нефрэктомия.
Декапсуляция почки — удаление фиброзной капсулы с целью устранения сдавления почечной паренхимы Применяется главным образом при остром гнойном воспалении почек (гнойный пиелонефрит, апостематозный нефрит, карбункул почки). Эту операцию часто сочетают с нефростомией, реже с пиелостомией — создание наружных свищей соответственно на почке или лоханке с целью их дренирования.
Нефротомию — рассечение паренхимы почки — производят с целью осмотра паренхимы, лоханки, их дренирования или извлечения конкрементов а также для выполнения нефростомии. Разрез производят поперек длинной оси почки (поперечная нефротомия) или по выпуклому, латеральному краю почки до лоханки (секционная нефротомия).
Резекция почки (удаление части почки , обычно одного из ее полюсов, реже средней части) осуществляется при повреждении почечной паренхимы, очаговых патологических процессах (туберкулезе почки , опухоли единственной почки и др.), солитарной кисте, форникально-чашечном кровотечении.
Нефрэктомию, т.е. удаление почки, производят при злокачественных опухолях, обширных повреждениях почки , гидронефрозе, нефрогенной артериальной гипертензии в связи с поражением одной почки, в случаях неэффективности других способов лечения при гнойном воспалении почки. Билатеральная нефрэктомия является промежуточным этапом трансплантации почек.
Библиогр.: Гарин А.М. и Алиев Д.А. Лечение диссеминированных форм злокачественных новообразований, с. 203, Баку, 1988; Клиническая нефрология, под ред. Е.М. Тареева, т. 1, М., 1983; Клиническая онкоурология, под ред. Е.Б. Мариибаха, с. 5, М., 1975; Лопаткин Н.А. и Пугачев А.Г. Детская урология, М., 1986; Люлько А.В., Мурванидзе Д.Д. и Возианов А.Ф. Основы практической урологии детского возраста, Киев, 1984; Мухин Н.Д. и Тареева И.Е. Диагностика и лечение болезней почек, М, 1985, библиогр.; Пытель Ю.А. и Золотарев И.И. Неотложная урология, М., 1985: они же. Ошибки и осложнения при рентгенологическом исследовании почек и мочевых путей, М., 1987; Терещенко А.В. и Люлько А.В. Рентгеноурологическая диагностика в педиатрии, Киев, 1985; Трапезникова М.Ф. Опухоли почек, М., 1978, библиогр.; Устименко Е.М. Травма почек, М., 1981, библиогр.